BCMB30004 CELL SIGNALLING & NEUROCHEMISTRY Semester 2, 2021
Hello, dear friend, you can consult us at any time if you have any questions, add WeChat: daixieit
BIOCHEMISTRY & MOLECULAR BIOLOGY
BCMB30004
Section A (19 marks)
Section A Question 1 (9 marks)
The neurocytokinin family of proteins activate c-Src kinase. Sequence deletion and mutagenesis experiments have found a region of the neurocytokinin (NCK) sequences that plays a critical role in activation. The alignment of these regions is:
NCK1 SDIQRSLYDQPASAK
NCK2 GPLDGSLYDNVKKKD
NCK3 SSEPVGIYQEFEKKT
NCK4 ERFLFPEYNEDPEPQ
i) Describe the domain organization and structure of inactive c-Src kinase. (5 marks)
ii) Using the information provided propose a mechanism for how a neurocytokinin activates c-Src kinase. (4 marks)
Section A Question 2 (6 marks)
In a model of inflammatory bowel disease using a gut cell line, the over-expression of a histone deacetylase relieves corticosteroid resistance. Propose mechanisms to explain why the cells showed resistance to corticosteroid and why over-expression of a histone deacetylase relieves resistance.
Section A Question 3 (4 marks)
A small molecule screen identifies a novel ligand that binds specifically to the glucocorticoid nuclear receptor. Testing the ability of the ligand to signal indicates that the novel ligand switches on glucocorticoid nuclear receptor signalling within several seconds. Propose a signalling mechanism and justify your reasoning.
Section B (19 marks)
Section B Question 4 (19 marks)
The peptide hormone/neuromodulator neurotensin mediates its actions mainly through binding and activating the Gq-coupled receptor, NTSR1.
i) Describe one assay that could be used to measure neurotensin-induced NTSR1 signalling.
(4 marks)
The following information is required to answer questions ii) and iii).
Structural and molecular pharmacological studies have revealed that neurotensin binds to NTSR1 mainly through the C-terminal amino acids tyrosine 11 (Tyr11, Y11), isoleucine 12 and leucine 13 of the peptide (Figure A below). A graduate researcher has synthesised a modified neurotensin peptide where the hydroxy group of Tyr11 (Figure A) is replaced with a much bulkier substituent (approx. four times the molecular mass of OH).
The graduate researcher conducts an experiment to test the modified peptide on the wild- type NTSR1 receptor, as well as a stabilised NTSR1 mutant receptor. The results of the experiment are depicted in Figure B.
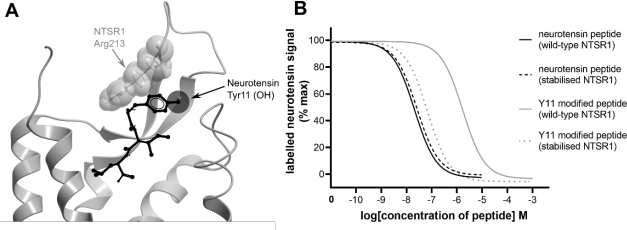
ii) What sort of experiment is depicted in Figure B and what key measure of peptide action can be determined from the curves? (2 marks)
iii) Describe how the Tyr11 modified peptide behaves on both receptors compared to the unmodified neurotensin peptide. (4 marks)
The following information is required to answer questions iv) and v).
The stabilised NTSR1 receptor used in the experiment above contains several mutations, including one at position 213, which is an arginine in the wild-type receptor (Figure A). The stabilised NTSR1 receptor also exhibits increased basal signalling (i.e. it exhibits constitutive activity) compared to the wild-type receptor.
iv) Based on this information, form a hypothesis as to why the Tyr11 modified peptide behaves as it does in Figure B. (4 marks)
v) Propose an experiment, with controls, that seeks to test your hypothesis. (5 marks)
Section C (36 marks)
Section C Question 5 (10 marks)
Design a proteolysis-targeting chimera (PROTAC) to enhance cell survival.
(i) How do PROTACs work? (2 marks)
(ii) What does your PROTAC target? List a cell death pathway that involves your target and outline the steps resulting in death by this pathway. (4 marks)
(iii) Which drug would be the most useful to test if your PROTAC is working as designed:
chloroquine, rapamycin or MG132? Why? (2 marks)
(iv) What morphological changes are expected in untreated and PROTAC-treated cells when death is triggered as in (ii). (2 marks)
Section C Question 6 (10 marks)
MARCH1 is a RING E3 ubiquitin ligase. It regulates levels of transferrin receptor in the plasma membrane.
(i) What is the fate of ubiquitinated transferrin receptor? (1 mark)
(ii) Describe the machinery involved in regulating levels of plasma membrane ubiquitinated transferrin receptor. (3 marks)
(iii) Which of the following drugs would most likely increase transferrin receptor expression: chloroquine, rapamycin or MG132? Why? (2 marks)
(iv) Provide two examples of how plasma membrane transferrin receptor levels could be
altered by treatment with drugs that activate deubiquitinases (DUBs). In your answer identify specific DUBs and indicate whether the drug would increase or decrease transferrin receptor plasma membrane levels. (4 marks)
Section C Question 7 (8 marks)
Mitochondrial damage can elicit neurodegenerative disease.
(i) Describe the mechanisms of ubiquitin-mediated regulation of mitochondrial health. (6 marks)
(ii) Based on your knowledge of (i) what is an effective clinical strategy to enhance
mitochondrial health in neurodegenerative disease? (2 marks)
Section C Question 8 (8 marks)
(i) Describe selective autophagy using an example from neurodegenerative disease. (3 marks)
(ii) In the scenarios below, predict whether levels of p62 increase, decrease or remain unchanged compared to control siRNA-treated cells that are not treated in any other way. Control cells are undergoing low levels of autophagy. Measurements are made under conditions where cells have been treated with chloroquine. siRNA reduces the expression of genes. (1 mark each, 5 marks total)
(a) siRNA knockdown of AMPK in cells that have high ATP.
(b) siRNA knockdown of TSC1.
(c) Control siRNA-treated cells treated with a drug that activates chaperone-mediated autophagy.
(d) Control siRNA-treated cells treated with rapamycin. (e) siRNA knockdown of TSC2.
Section D (15 marks)
Section D Question 9 (15 marks)
Researchers are trying to develop a vaccine against a virus that attacks the brain. They find that immunising mice with the vaccine via an intramuscular injection is ineffective at preventing the virus infecting and damaging brain tissue. Describe THREE (3) approaches that target structures and/or molecules associated with the brain that may increase effectiveness of an intramuscular vaccine against the virus in the brain. Each approach must target a different structure and/or molecule. Your answers must explain the mechanisms that underpin each approach. (15 marks, 5 marks per approach)
Section E (31 marks)
Section E Question 10 (23 marks)
While traveling in the outback, Sally was bitten by a spider that immediately caused a sharp, localised pain. She managed to catch the spider and discovered that it was a new species. She sought to understand the mechanisms behind its pain-promoting functions, so she prepared an extract of the spider venom.
Sally isolated neurons from the dorsal root ganglia (DRG) of mice and grew them in culture. Using electrophysiology and whole-cell patch clamp recording, she observed the following effects on membrane excitability after exposure to vehicle or extract:
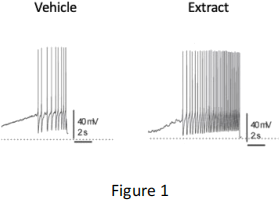
i) Based on these results (Figure 1), name three types of pain receptors (from different families/classes) that could be the target of the venom and whether they would be activated or inhibited by the venom. Explain your reasoning. (6 marks)
ii) Predict how the rheobase of the DRG neurons would change upon exposure to the venom extract. Explain your reasoning. (2 marks)
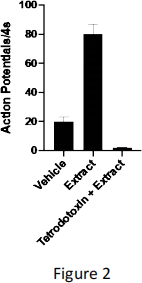
iii) Next, Sally studied the effect of the venom extract on action potential firing rate before and after pre-treatment with tetrodotoxin (Figure 2). Based on these data, name a pain mediator in primary nociceptors that can be excluded as the target of the venom extract and why? (2 marks)
iv) Sally next pre-treated the DRG neurons with Dy4 (an inhibitor of dynamin-dependent endocytosis) prior to adding the extract. Using the information above, predict what effect this will have on action potential frequency and amplitude. Explain your reasoning. (3 marks)
v) Design two simple experiments (using different techniques) that would help to confirm the identity of the spider venom’s target. State the controls you would use, the possible outcomes of these experiments and how they would be interpreted. (10 marks)
Section E Question 11 (8 marks)
Like PAR2 and NK1R, opioid receptors can be internalised into endosomes upon activation. In an attempt to study the effects of endosomal opioid receptor signalling on pain, researchers developed a nanoparticle system that can deliver opioid agonists to both the cell surface and endosomes (Nano-Ag). The nanoparticles were then tested in two experiments in comparison to vehicle (no agonist) or free agonist that targets only the cell surface receptors (Ag).
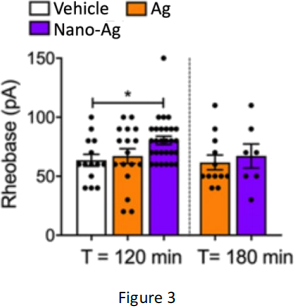
i) In the first experiment (Figure 3), cultured primary neurons were exposed to vehicle, Ag or Nano-Ag for 120 or 180 minutes, after which rheobase was measured by patch-clamp recording. Summarise the outcomes of this experiment and interpret the results. (2 marks)
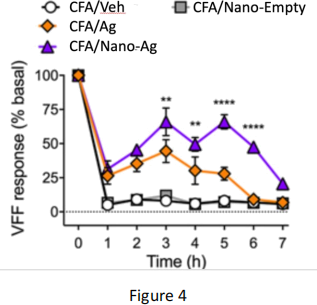
ii) In the second experiment (Figure 4), the effects of opioid activation were examined in an inflammatory pain model in whole mice. Baseline withdrawal thresholds were measured in mouse paws using von Frey filaments (t=0) and then the paws were injected with an agent called CFA that is known to cause inflammatory pain. After 48 hours, mice were randomised into 4 groups and paws were injected with the following: vehicle, Ag, Nano- Ag, or empty nanoparticles (Nano-Empty). Withdrawal thresholds were then measured hourly over the next 7 hours. Summarise the outcomes of this experiment and interpret the results. (4 marks)
iii) How could these results inform drug development strategies for the treatment of pain?
(2 marks)
2021-12-10