ENGR 145 Practice 1
Hello, dear friend, you can consult us at any time if you have any questions, add WeChat: daixieit
1) For each of the following scenarios, explain the mathematical approach of the nodes on the ψσ and ψσ* MOs.
a. s and s orbital overlap
b. s and p orbital overlap
c. p and p orbital overlap
2) For the O2 molecule, draw the atomic and molecular orbitals and identify: (i) all anti-bonding orbitals (ii) HOMO and LUMO (iii) bond order (iv) which atom has lower energy orbitals (v) which atom the bonding MO is more similar to
3) The molecular structure of phenylalanine is shown below:
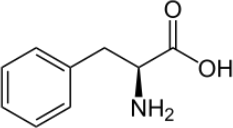
a. Draw the molecular structure with all C and H atoms shown
b. Identify the hybridization of every C atom
c. True/False: This atom has stronger double bonds that alternate with weaker single bonds every other carbon
d. Are there localized π e-? Delocalized π e-?
e. What is the orientation of the p orbitals in the π bonds?
4) The molecular structure of β-carotene is shown below:
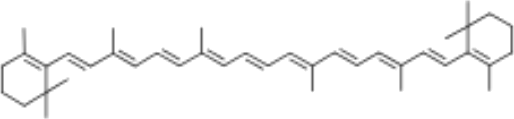
a. Are there localized π e-? Delocalized π e-
b. Sketch a “true” representation of the double bonds on the backbone of this molecule (hint: think about bond order)
5) On the energy band diagrams below:
a. Draw the occupancy of electrons
b. Identify the band gap (if present)
c. Determine if the element is a conductor or insulator/semiconductor
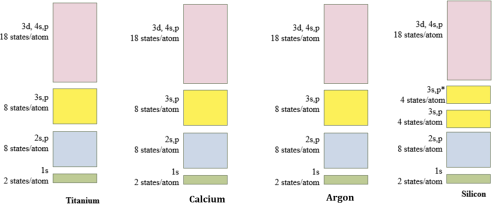
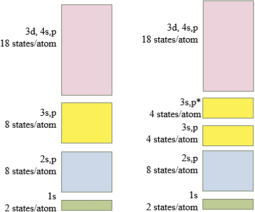
6) Suppose you didn’t know which of the two band diagrams better described aluminum. In each case, draw the occupancy of electrons, identify the band gap (if present), and determine whether the analysis suggests aluminum is a conductor or insulator/semiconductor.
7) Rank the following semiconductors in order of band gap size: Si, GaSe, InTe, AlP, Ge
2023-07-11